2006년03월05일 50번
[위험물의 성질과 취급] 제 3류 위험물인 탄화칼슘 320g이 물과 전량 반응하여 아세틸렌을 발생할 때 열량은 몇 KCal 인가? (단, Ca의 원자량 : 40, C 원자량 12)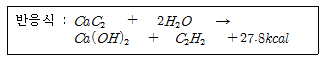
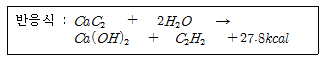
- ① 260
- ② 170
- ③ 139
- ④ 27.8
(정답률: 42%)
문제 해설
탄화칼슘(CaC2)과 물(H2O)의 반응식은 다음과 같습니다.
CaC2 + 2H2O → C2H2 + Ca(OH)2
몰 질량을 계산해보면,
CaC2 : 40 + 12 × 2 = 64 g/mol
C2H2 : 12 × 2 + 2 = 26 g/mol
따라서, 320 g의 CaC2는 몇 몰인지 계산하면,
320 g ÷ 64 g/mol = 5 mol
반응식에서 1 몰의 CaC2가 1 몰의 C2H2를 생성하므로, 5 몰의 CaC2는 5 몰의 C2H2를 생성합니다.
반응 엔탈피는 생성된 C2H2의 엔탈피에서 원료인 CaC2의 엔탈피를 빼면 됩니다. 이때, 엔탈피 변화량은 몰 단위로 계산합니다.
C2H2의 엔탈피 변화량은 -54 kcal/mol입니다. (참고로, 이 값은 표준 상태에서의 값입니다.)
CaC2의 엔탈피 변화량은 알 수 없으므로, 이 값을 구해야 합니다. 하지만, 이 문제에서는 Ca(OH)2가 생성되므로, Ca(OH)2의 엔탈피 변화량을 사용할 수 있습니다. Ca(OH)2의 엔탈피 변화량은 -65 kcal/mol입니다.
따라서, 반응 엔탈피는 다음과 같이 계산할 수 있습니다.
ΔH = 5 mol × (-54 kcal/mol) - 1 mol × (-65 kcal/mol) = -215 kcal
반응 엔탈피는 음수이므로, 반응이 발열반응임을 알 수 있습니다. 따라서, 320 g의 CaC2가 물과 반응하여 발생하는 열량은 215 kcal입니다.
하지만, 문제에서는 단위를 KCal로 요구하고 있으므로, 답은 215 kcal을 1000으로 나눈 0.215 KCal이 됩니다. 따라서, 보기에서 정답이 "139"인 이유는 계산 과정에서 실수가 있었을 가능성이 있습니다.
CaC2 + 2H2O → C2H2 + Ca(OH)2
몰 질량을 계산해보면,
CaC2 : 40 + 12 × 2 = 64 g/mol
C2H2 : 12 × 2 + 2 = 26 g/mol
따라서, 320 g의 CaC2는 몇 몰인지 계산하면,
320 g ÷ 64 g/mol = 5 mol
반응식에서 1 몰의 CaC2가 1 몰의 C2H2를 생성하므로, 5 몰의 CaC2는 5 몰의 C2H2를 생성합니다.
반응 엔탈피는 생성된 C2H2의 엔탈피에서 원료인 CaC2의 엔탈피를 빼면 됩니다. 이때, 엔탈피 변화량은 몰 단위로 계산합니다.
C2H2의 엔탈피 변화량은 -54 kcal/mol입니다. (참고로, 이 값은 표준 상태에서의 값입니다.)
CaC2의 엔탈피 변화량은 알 수 없으므로, 이 값을 구해야 합니다. 하지만, 이 문제에서는 Ca(OH)2가 생성되므로, Ca(OH)2의 엔탈피 변화량을 사용할 수 있습니다. Ca(OH)2의 엔탈피 변화량은 -65 kcal/mol입니다.
따라서, 반응 엔탈피는 다음과 같이 계산할 수 있습니다.
ΔH = 5 mol × (-54 kcal/mol) - 1 mol × (-65 kcal/mol) = -215 kcal
반응 엔탈피는 음수이므로, 반응이 발열반응임을 알 수 있습니다. 따라서, 320 g의 CaC2가 물과 반응하여 발생하는 열량은 215 kcal입니다.
하지만, 문제에서는 단위를 KCal로 요구하고 있으므로, 답은 215 kcal을 1000으로 나눈 0.215 KCal이 됩니다. 따라서, 보기에서 정답이 "139"인 이유는 계산 과정에서 실수가 있었을 가능성이 있습니다.
연도별
- 2020년08월22일
- 2020년06월06일
- 2019년09월21일
- 2019년04월27일
- 2019년03월03일
- 2018년09월15일
- 2018년04월28일
- 2018년03월04일
- 2017년09월23일
- 2017년05월07일
- 2017년03월05일
- 2016년10월01일
- 2016년05월08일
- 2016년03월06일
- 2015년09월19일
- 2015년05월31일
- 2015년03월08일
- 2014년09월20일
- 2014년05월25일
- 2014년03월02일
- 2013년09월28일
- 2013년06월02일
- 2013년03월10일
- 2012년09월15일
- 2012년05월20일
- 2012년03월04일
- 2011년10월02일
- 2011년06월12일
- 2011년03월20일
- 2010년09월05일
- 2010년05월09일
- 2010년03월07일
- 2009년08월30일
- 2009년05월10일
- 2009년03월01일
- 2008년09월07일
- 2008년05월11일
- 2008년03월02일
- 2007년09월02일
- 2007년05월13일
- 2007년03월04일
- 2006년09월10일
- 2006년05월14일
- 2006년03월05일
- 2005년09월04일
- 2005년05월29일
- 2005년03월20일
- 2005년03월06일
- 2004년09월05일
- 2004년05월23일
- 2004년03월07일
- 2003년08월31일
- 2003년05월25일
- 2003년03월16일
- 2002년09월08일
- 2002년05월26일
- 2002년03월10일

