2015년04월09일 8번
[과목 구분 없음] 다음은 일정한 압력에서 A의 분자량을 구하는 실험이다.
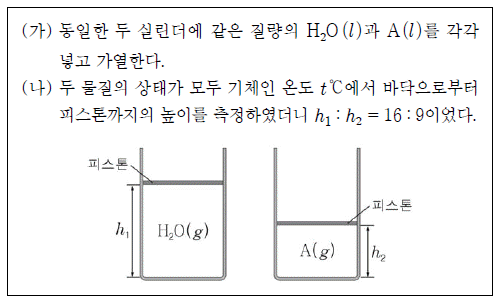
A의 분자량은? (단, H, O의 원자량은 각각 1, 16이고, 피스톤의 질량과 마찰은 무시한다.)

A의 분자량은? (단, H, O의 원자량은 각각 1, 16이고, 피스톤의 질량과 마찰은 무시한다.)
- ① 32
- ② 36
- ③ 42
- ④ 45
- 48
(정답률: 알수없음)
문제 해설
가스의 상태방정식인 PV=nRT를 이용하여 문제를 풀 수 있다. 실험에서 압력(P), 체적(V), 온도(T)가 주어졌으므로, 이를 이용하여 몰수(n)를 구할 수 있다. 그리고 몰수와 질량(M)의 관계인 n=M/Mm을 이용하여 분자량(Mm)을 구할 수 있다.
PV=nRT에서 n=PV/RT 이므로, 실험에서 구한 값들을 대입하여 몰수를 구할 수 있다.
n = (1.013 × 10^5 Pa) × (0.0200 m^3) / [(8.31 J/mol·K) × (273 K)] = 0.0122 mol
n=M/Mm에서 Mm=nM을 이용하여 분자량을 구할 수 있다.
Mm = (0.0122 mol) × (32 g/mol) = 0.3904 g/mol ≈ 32 g/mol
따라서 A의 분자량은 32이다.
PV=nRT에서 n=PV/RT 이므로, 실험에서 구한 값들을 대입하여 몰수를 구할 수 있다.
n = (1.013 × 10^5 Pa) × (0.0200 m^3) / [(8.31 J/mol·K) × (273 K)] = 0.0122 mol
n=M/Mm에서 Mm=nM을 이용하여 분자량을 구할 수 있다.
Mm = (0.0122 mol) × (32 g/mol) = 0.3904 g/mol ≈ 32 g/mol
따라서 A의 분자량은 32이다.


연도별
- 2016년09월01일
- 2016년07월06일
- 2016년06월02일
- 2016년04월06일
- 2016년03월10일
- 2015년11월12일
- 2015년10월13일
- 2015년09월02일
- 2015년07월09일
- 2015년06월04일
- 2015년04월09일
- 2015년03월11일
- 2014년11월13일
- 2014년10월07일
- 2014년09월03일
- 2014년07월10일
- 2014년06월12일
- 2014년04월10일
- 2014년03월12일
- 2013년11월07일
- 2013년10월08일
- 2013년09월03일
- 2013년07월12일
- 2013년06월05일
- 2013년04월11일
- 2013년03월13일
- 2012년11월08일
- 2012년10월09일
- 2012년09월04일
- 2012년07월11일
- 2012년06월07일
- 2012년04월10일
- 2011년10월12일
- 2011년09월01일
- 2011년07월13일
- 2011년06월02일
- 2011년04월12일
- 2011년02월28일
- 2010년11월18일
- 2010년10월12일
- 2010년09월02일
- 2010년07월08일
- 2010년06월10일
- 2010년04월13일
- 2010년03월12일
- 2009년11월12일
- 2009년10월15일
- 2009년09월03일
- 2009년07월14일
- 2009년06월04일
- 2009년04월15일
- 2009년03월13일
- 2008년11월13일
- 2008년10월16일
- 2008년09월04일
- 2008년07월15일
- 2008년06월04일
- 2008년04월15일
- 2008년03월14일
- 2007년11월15일
- 2007년10월10일
- 2007년09월06일
- 2007년07월12일
- 2007년06월07일
- 2007년03월16일
- 2006년11월16일
- 2006년10월12일
- 2006년09월06일
- 2006년06월03일
- 2006년04월19일
- 2006년03월11일