2020년09월26일 59번
[화학물질 구조분석] 니켈(Ni2+)과 카드뮴(Cd2+)이 각각 0.1M인 혼합용액에서 니켈만 전기화학적으로 석출하고자 한다. 카드뮴이온은 석출되지 않고, 니켈이온이 0.01%만 남도록 하는 전압(V)은?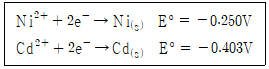
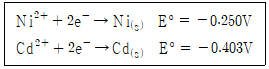
- ① -0.2
- ② -0.3
- ③ -0.4
- ④ -0.5
(정답률: 30%)
문제 해설
전기화학적 석출은 전극에 전압을 가해 전해질을 분해하여 원소로 변화시키는 과정이다. 이 문제에서는 니켈만 전기화학적으로 석출하고자 하므로, 니켈의 전극 반응을 이용하여 전압을 구할 수 있다.
니켈의 전극 반응은 Ni2+ + 2e- → Ni 이다. 이 반응에서 전자 2개가 전극으로 이동하여 니켈 이온이 원자로 변화하고, 이 과정에서 전극에 전압이 발생한다.
니켈이온의 농도가 0.1M이므로, 이온의 활동도는 농도와 같다. 따라서 Ni2+의 활동도는 0.1이다. 니켈이온의 활동도가 0.01%만 남도록 하려면, 전극 반응에서 전자 2개가 전해질로 이동할 때 발생하는 전압이 일정 수준 이상이어야 한다.
전극 반응에서 발생하는 전압은 Nernst 방정식을 이용하여 구할 수 있다. Nernst 방정식은 E = E0 - (RT/nF)lnQ 이다. 여기서 E는 전극 반응에서 발생하는 전압, E0은 표준 전극전위, R은 기체 상수, T는 절대온도, n은 전자의 수, F는 Faraday 상수, Q는 반응의 활성도곱이다.
이 문제에서는 니켈만 전기화학적으로 석출하므로, 반응의 활성도곱은 Ni2+의 활동도와 같다. 따라서 Q = [Ni2+] = 0.1이다. 전자의 수는 2이고, 표준 전극전위는 표준수소전극을 기준으로 정해진다. Ni2+ + 2e- → Ni 반응의 표준전극전위는 -0.25V이다.
따라서, E = -0.25 - (0.0257/2)ln(0.001) = -0.4V 이다. 따라서 정답은 "-0.4"이다.
니켈의 전극 반응은 Ni2+ + 2e- → Ni 이다. 이 반응에서 전자 2개가 전극으로 이동하여 니켈 이온이 원자로 변화하고, 이 과정에서 전극에 전압이 발생한다.
니켈이온의 농도가 0.1M이므로, 이온의 활동도는 농도와 같다. 따라서 Ni2+의 활동도는 0.1이다. 니켈이온의 활동도가 0.01%만 남도록 하려면, 전극 반응에서 전자 2개가 전해질로 이동할 때 발생하는 전압이 일정 수준 이상이어야 한다.
전극 반응에서 발생하는 전압은 Nernst 방정식을 이용하여 구할 수 있다. Nernst 방정식은 E = E0 - (RT/nF)lnQ 이다. 여기서 E는 전극 반응에서 발생하는 전압, E0은 표준 전극전위, R은 기체 상수, T는 절대온도, n은 전자의 수, F는 Faraday 상수, Q는 반응의 활성도곱이다.
이 문제에서는 니켈만 전기화학적으로 석출하므로, 반응의 활성도곱은 Ni2+의 활동도와 같다. 따라서 Q = [Ni2+] = 0.1이다. 전자의 수는 2이고, 표준 전극전위는 표준수소전극을 기준으로 정해진다. Ni2+ + 2e- → Ni 반응의 표준전극전위는 -0.25V이다.
따라서, E = -0.25 - (0.0257/2)ln(0.001) = -0.4V 이다. 따라서 정답은 "-0.4"이다.
연도별
진행 상황
0 오답
0 정답

