2021년03월07일 25번
[화학물질 특성분석] 0.04M Na3PO4용액의 pH는? (단, 인산의 Ka는 4.5×10-13 이다.)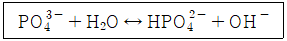
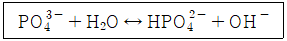
- ① 8.43
- ② 10.32
- ③ 12.32
- ④ 13.32
(정답률: 47%)
문제 해설
Na3PO4는 염기성 염이므로 수용액은 염기성일 것이다. 따라서 pH는 7보다 높을 것이다.
Na3PO4는 Na+와 PO43- 이온으로 이루어져 있으며, PO43- 이온은 염기성을 띠고 있다. PO43- 이온은 수용액에서 다음과 같은 평형 반응을 일으킨다.
PO43- + H2O ⇌ HPO42- + OH-
이 평형 상수는 Kb = 2.3 × 10-2 이다.
PO43- 이온의 농도를 계산하기 위해 Na3PO4의 몰농도를 계산한다.
0.04 M Na3PO4 용액에서 PO43- 이온의 몰농도는 0.04 M 이다.
PO43- 이온의 농도를 이용하여 OH- 이온의 농도를 계산한다.
Kb = [HPO42-][OH-]/[PO43-]
2.3 × 10-2 = x2/0.04
x = 0.096 M
따라서 OH- 이온의 농도는 0.096 M 이다.
pOH = -log[OH-] = -log(0.096) = 1.02
pH = 14 - pOH = 12.32
따라서 정답은 "12.32" 이다.
Na3PO4는 Na+와 PO43- 이온으로 이루어져 있으며, PO43- 이온은 염기성을 띠고 있다. PO43- 이온은 수용액에서 다음과 같은 평형 반응을 일으킨다.
PO43- + H2O ⇌ HPO42- + OH-
이 평형 상수는 Kb = 2.3 × 10-2 이다.
PO43- 이온의 농도를 계산하기 위해 Na3PO4의 몰농도를 계산한다.
0.04 M Na3PO4 용액에서 PO43- 이온의 몰농도는 0.04 M 이다.
PO43- 이온의 농도를 이용하여 OH- 이온의 농도를 계산한다.
Kb = [HPO42-][OH-]/[PO43-]
2.3 × 10-2 = x2/0.04
x = 0.096 M
따라서 OH- 이온의 농도는 0.096 M 이다.
pOH = -log[OH-] = -log(0.096) = 1.02
pH = 14 - pOH = 12.32
따라서 정답은 "12.32" 이다.
연도별
진행 상황
0 오답
0 정답

