2016년06월02일 20번
[과목 구분 없음] 다음은 기체 A가 분해되는 반응의 화학 반응식이다.
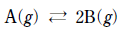
그림에서 (가)는 온도 T, 압력 P, 부피 V 에서 기체 A와 B가 평형을 이루고 있는 상태를, (나)와 (다)는 (가)에서 순차적으로 조건을 달리하여 새롭게 도달한 평형 상태를 나타낸 것이다.
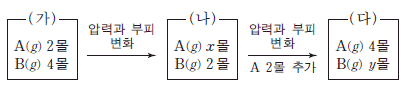
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 온도는 일정하다.) [3점]
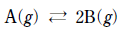
그림에서 (가)는 온도 T, 압력 P, 부피 V 에서 기체 A와 B가 평형을 이루고 있는 상태를, (나)와 (다)는 (가)에서 순차적으로 조건을 달리하여 새롭게 도달한 평형 상태를 나타낸 것이다.
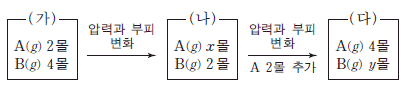
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 온도는 일정하다.) [3점]

- ① ㄱ
- ② ㄴ
- ③ ㄷ
- ④ ㄱ, ㄷ
- ⑤ ㄴ, ㄷ
(정답률: 알수없음)
문제 해설
보기에서 정답은 "ㄴ, ㄷ"이다.
- (ㄱ)은 온도가 변하지 않았기 때문에 기체 A와 B의 분해와 합성 속도가 일정하게 유지되어 평형 상태가 변하지 않는다는 것이다. 하지만 그림에서 (가)와 (나)를 비교해보면 압력이 증가하면 기체 B의 분해 속도가 증가하여 기체 A의 농도가 감소하고, 부피가 감소하면 기체 A와 B의 농도가 모두 증가한다는 것을 알 수 있다. 따라서 (ㄱ)은 옳지 않다.
- (ㄴ)은 압력이 증가하면 기체 B의 분해 속도가 증가하여 기체 A의 농도가 감소하고, 부피가 감소하면 기체 A와 B의 농도가 모두 증가한다는 것을 그림에서 확인할 수 있다. 따라서 (ㄴ)은 옳다.
- (ㄷ)는 압력이 감소하면 기체 B의 합성 속도가 증가하여 기체 A의 농도가 증가하고, 부피가 증가하면 기체 A와 B의 농도가 모두 감소한다는 것을 그림에서 확인할 수 있다. 따라서 (ㄷ)은 옳다.
- (ㄱ, ㄷ)는 이미 (ㄱ)과 (ㄷ)가 각각 옳은 것으로 판명되었기 때문에 모순된다.
- 따라서 정답은 "ㄴ, ㄷ"이다.
- (ㄱ)은 온도가 변하지 않았기 때문에 기체 A와 B의 분해와 합성 속도가 일정하게 유지되어 평형 상태가 변하지 않는다는 것이다. 하지만 그림에서 (가)와 (나)를 비교해보면 압력이 증가하면 기체 B의 분해 속도가 증가하여 기체 A의 농도가 감소하고, 부피가 감소하면 기체 A와 B의 농도가 모두 증가한다는 것을 알 수 있다. 따라서 (ㄱ)은 옳지 않다.
- (ㄴ)은 압력이 증가하면 기체 B의 분해 속도가 증가하여 기체 A의 농도가 감소하고, 부피가 감소하면 기체 A와 B의 농도가 모두 증가한다는 것을 그림에서 확인할 수 있다. 따라서 (ㄴ)은 옳다.
- (ㄷ)는 압력이 감소하면 기체 B의 합성 속도가 증가하여 기체 A의 농도가 증가하고, 부피가 증가하면 기체 A와 B의 농도가 모두 감소한다는 것을 그림에서 확인할 수 있다. 따라서 (ㄷ)은 옳다.
- (ㄱ, ㄷ)는 이미 (ㄱ)과 (ㄷ)가 각각 옳은 것으로 판명되었기 때문에 모순된다.
- 따라서 정답은 "ㄴ, ㄷ"이다.
이전 문제
다음 문제
연도별
- 2016년11월17일
- 2016년10월11일
- 2016년09월01일
- 2016년07월06일
- 2016년06월02일
- 2016년04월06일
- 2015년11월12일
- 2015년10월13일
- 2015년09월02일
- 2015년07월09일
- 2015년06월04일
- 2015년04월09일
- 2014년11월13일
- 2014년10월07일
- 2014년09월03일
- 2014년07월10일
- 2014년06월12일
- 2014년04월10일
- 2013년11월07일
- 2013년10월08일
- 2013년09월03일
- 2013년07월12일
- 2013년06월05일
- 2013년04월11일
- 2012년11월08일
- 2012년10월09일
- 2012년09월04일
- 2012년07월11일
- 2012년06월07일
- 2012년04월10일
- 2011년10월12일
- 2011년09월01일
- 2011년07월13일
- 2011년06월02일
- 2011년04월12일
- 2010년11월18일
- 2010년10월12일
- 2010년09월02일
- 2010년07월08일
- 2010년06월10일
- 2010년04월13일
- 2009년11월12일
- 2009년10월15일
- 2009년09월03일
- 2009년07월14일
- 2009년06월04일
- 2009년04월15일
- 2008년11월13일
- 2008년10월16일
- 2008년09월04일
- 2008년07월15일
- 2008년06월04일
- 2008년04월15일
- 2007년11월15일
- 2007년10월10일
- 2007년09월06일
- 2007년07월12일
- 2007년06월07일
- 2007년04월18일
- 2006년11월16일
- 2006년10월12일
- 2006년09월06일
- 2006년06월03일
- 2006년04월19일

