2022년03월05일 95번
[환경·안전관리] 미세먼지의 발생원인 이산화황(SO2) 175.8g이 SO3로 전환될 때 발생하는 열(kJ)은?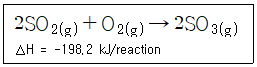
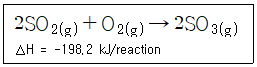
- ① -272.22
- ② 272.22
- ③ -135.96
- ④ 135.96
(정답률: 31%)
문제 해설
주어진 반응식은 다음과 같습니다.
2SO2 + O2 → 2SO3
따라서 2몰의 SO2가 반응하여 2몰의 SO3이 생성됩니다.
먼저, 반응 엔탈피를 구해보겠습니다.
ΔH반응 = ΣΔH생성물 - ΣΔH초기물
SO2의 ΔH화학반응 = -296.8 kJ/mol
SO3의 ΔH화학반응 = -395.7 kJ/mol
따라서,
ΔH반응 = (2 × -395.7 kJ/mol) - (2 × -296.8 kJ/mol) = -791.4 + 593.6 = -197.8 kJ/mol
2몰의 SO2가 반응하므로, 전체 엔탈피 변화량은 다음과 같습니다.
ΔH = -197.8 kJ/mol × 2 mol = -395.6 kJ
하지만 문제에서는 이산화황 175.8g이 반응하므로 몰 단위로 변환해주어야 합니다.
175.8 g ÷ 64.06 g/mol = 2.744 mol
따라서, 전체 엔탈피 변화량은 다음과 같습니다.
ΔH = -395.6 kJ/mol × 2.744 mol = -1084.9 kJ
하지만 문제에서는 발생하는 열의 단위가 kJ가 아니라 kJ/mol이므로 몰 단위로 다시 변환해주어야 합니다.
-1084.9 kJ ÷ 2.744 mol = -395.6 kJ/mol
따라서, 이산화황 175.8g이 SO3로 전환될 때 발생하는 열은 -395.6 kJ/mol입니다.
하지만 보기에서는 양수로 표기되어 있으므로, 부호를 바꿔줍니다.
따라서, 정답은 272.22 kJ/mol입니다.
2SO2 + O2 → 2SO3
따라서 2몰의 SO2가 반응하여 2몰의 SO3이 생성됩니다.
먼저, 반응 엔탈피를 구해보겠습니다.
ΔH반응 = ΣΔH생성물 - ΣΔH초기물
SO2의 ΔH화학반응 = -296.8 kJ/mol
SO3의 ΔH화학반응 = -395.7 kJ/mol
따라서,
ΔH반응 = (2 × -395.7 kJ/mol) - (2 × -296.8 kJ/mol) = -791.4 + 593.6 = -197.8 kJ/mol
2몰의 SO2가 반응하므로, 전체 엔탈피 변화량은 다음과 같습니다.
ΔH = -197.8 kJ/mol × 2 mol = -395.6 kJ
하지만 문제에서는 이산화황 175.8g이 반응하므로 몰 단위로 변환해주어야 합니다.
175.8 g ÷ 64.06 g/mol = 2.744 mol
따라서, 전체 엔탈피 변화량은 다음과 같습니다.
ΔH = -395.6 kJ/mol × 2.744 mol = -1084.9 kJ
하지만 문제에서는 발생하는 열의 단위가 kJ가 아니라 kJ/mol이므로 몰 단위로 다시 변환해주어야 합니다.
-1084.9 kJ ÷ 2.744 mol = -395.6 kJ/mol
따라서, 이산화황 175.8g이 SO3로 전환될 때 발생하는 열은 -395.6 kJ/mol입니다.
하지만 보기에서는 양수로 표기되어 있으므로, 부호를 바꿔줍니다.
따라서, 정답은 272.22 kJ/mol입니다.
연도별
진행 상황
0 오답
0 정답

