2005년08월07일 37번
[기계열역학] 600kPa, 300 K 상태의 알곤(argon) 기체 1kmol이 엔탈피가 일정한 과정을 거쳐 압력이 원래의 1.3 배가 되었다. 일반기체상수 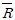 = 8.31451 kJ/kmolk 이다. 이 과정 동안 알곤(이상 기체)의 엔트로피 변화량은? (문제 오류로 정답이 정확하지 않습니다. 정답지를 찾지못하여 임의 정답 1번으로 설정하였습니다. 정답을 아시는 분께서는 오류 신고를 통하여 정답 입력 부탁 드립니다.)
= 8.31451 kJ/kmolk 이다. 이 과정 동안 알곤(이상 기체)의 엔트로피 변화량은? (문제 오류로 정답이 정확하지 않습니다. 정답지를 찾지못하여 임의 정답 1번으로 설정하였습니다. 정답을 아시는 분께서는 오류 신고를 통하여 정답 입력 부탁 드립니다.)
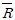 = 8.31451 kJ/kmolk 이다. 이 과정 동안 알곤(이상 기체)의 엔트로피 변화량은? (문제 오류로 정답이 정확하지 않습니다. 정답지를 찾지못하여 임의 정답 1번으로 설정하였습니다. 정답을 아시는 분께서는 오류 신고를 통하여 정답 입력 부탁 드립니다.)
= 8.31451 kJ/kmolk 이다. 이 과정 동안 알곤(이상 기체)의 엔트로피 변화량은? (문제 오류로 정답이 정확하지 않습니다. 정답지를 찾지못하여 임의 정답 1번으로 설정하였습니다. 정답을 아시는 분께서는 오류 신고를 통하여 정답 입력 부탁 드립니다.)- ① 0.782 kJ/K
- ② 8.31 kJ/K
- ③ 9.13 kJ/K
- ④ 60.0 kJ/K
(정답률: 알수없음)
문제 해설
알곤 기체가 이상 기체이므로, 이 과정에서 엔트로피 변화량은 다음과 같이 구할 수 있다.
ΔS = nRln(P2/P1) = (1 kmol)(8.31451 kJ/kmolK)ln(1.3) = 0.782 kJ/K
따라서, 정답은 "0.782 kJ/K"이다.
ΔS = nRln(P2/P1) = (1 kmol)(8.31451 kJ/kmolK)ln(1.3) = 0.782 kJ/K
따라서, 정답은 "0.782 kJ/K"이다.
연도별
- 2021년08월14일
- 2021년05월15일
- 2021년03월07일
- 2020년08월22일
- 2020년06월06일
- 2019년08월04일
- 2019년03월03일
- 2018년08월19일
- 2018년04월28일
- 2018년03월04일
- 2017년08월26일
- 2017년05월07일
- 2016년08월21일
- 2016년03월06일
- 2015년05월31일
- 2012년05월20일
- 2012년03월04일
- 2011년08월21일
- 2011년06월12일
- 2011년03월20일
- 2010년07월25일
- 2010년05월09일
- 2010년03월07일
- 2007년05월13일
- 2007년03월04일
- 2006년05월14일
- 2006년03월05일
- 2005년08월07일
- 2005년05월29일
- 2004년08월08일
- 2004년05월23일
- 2004년03월07일
- 2003년08월10일
- 2003년05월25일
- 2003년03월16일
진행 상황
0 오답
0 정답

