2019년04월27日 90번
[반응공학] 다음과 같은 1차 병렬 반응이 일정한 온도의 회분식 반응기에서 진행되었다. 반응시간이 1000s일 때 반응물 A가 90% 분해되어 생성물을 R이 S의 10배로 생성되었다. 반응초기에 R과 S의 농도를 0으로 할 때, k1 및 k1/k2은 각각 얼마인가?(오류 신고가 접수된 문제입니다. 반드시 정답과 해설을 확인하시기 바랍니다.)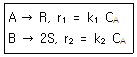
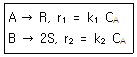
- ① k1=0.131/min, k1/k2=20
- ② k1=0.046/min, k1/k2=10
- ③ k1=0.131/min, k1/k2=10
- ④ k1=0.046/min, k1/k2=20
(정답률: 52%)
문제 해설
연도별
- 2021년08월14日
- 2021년05월15日
- 2021년03월07日
- 2020년09월26日
- 2020년08월22日
- 2020년06월06日
- 2019년09월21日
- 2019년04월27日
- 2019년03월03日
- 2018년09월15日
- 2018년04월28日
- 2018년03월04日
- 2017년09월23日
- 2017년05월07日
- 2017년03월05日
- 2016년10월01日
- 2016년05월08日
- 2016년03월06日
- 2015년09월19日
- 2015년05월31日
- 2015년03월08日
- 2014년09월20日
- 2014년05월25日
- 2014년03월02日
- 2013년09월28日
- 2013년03월10日
- 2012년05월20日
진행 상황
0 오답
0 정답


r1 = -k1[A]
r2 = -k2[A]
반응시간이 1000s일 때, A의 90%가 분해되어 R과 S가 생성되었으므로, A의 초기 농도를 [A]0라고 하면,
0.1[A]0 = [R] + [S]
또한, R과 S의 초기 농도는 0이므로,
[R] = 10[S]
따라서,
0.1[A]0 = 11[S]
[S] = 0.009[A]0
반응속도식은 다음과 같다.
d[A]/dt = -r1 - r2
d[A]/dt = k1[A] + k2[A]
d[A]/[A] = k1dt + k2dt
ln[A] - ln[A]0 = -(k1 + k2)t
ln[A]/[A]0 = -(k1 + k2)t
ln([A]0/[A]) = k1t + k2t
ln(1/0.1) = k11000 + k21000
ln(10) = 1000(k1 + k2)
k1 + k2 = ln(10)/1000
또한, R과 S의 농도 비율은 10:1 이므로, R과 S의 속도식은 다음과 같다.
rR = -k1[A]
rS = -k2[A]
따라서,
rR/rS = k1/k2
([R]/dt)/([S]/dt) = k1/k2
10[S]/[A] = k1/k2
10(0.009[A]0)/[A]0 = k1/k2
0.09 = k1/k2
따라서, k1과 k1/k2은 각각 0.131/min과 20이다.